- Planergia EkoMarketing
- Planergia Fotowoltaika
- Planergia Dotacje ▾
Wodór. Badania, sposób uzyskiwania, sposoby magazynowania, zalety wodoru jako paliwa, ogniwa paliwowe i silniki spalinowe.
Głównymi zaletami wodoru jako paliwa są:
-Wysoka wartość energetyczna (~120MJ/kg - ponad 4x więcej niż węgiel kamienny i ok. 3x więcej niż benzyna czy olej napędowy)
-Łatwość pozyskiwania
-Ochrona środowiska
Żyjemy w czasach, w których nieustannie rośnie zapotrzebowanie na energię, a jednocześnie dążymy do ochrony środowiska. Stosując wodór jako paliwo możemy uzyskać i jedno i drugie. Nastręcza nam to jednak pewnych trudności:
-Mały ciężar właściwy
-Mała objętościowa gęstość energii w porównaniu z paliwami kopalnymi
-Duża objętość zbiorników

Tabela 1 Wartości energii spalania wybranych paliw. (1)
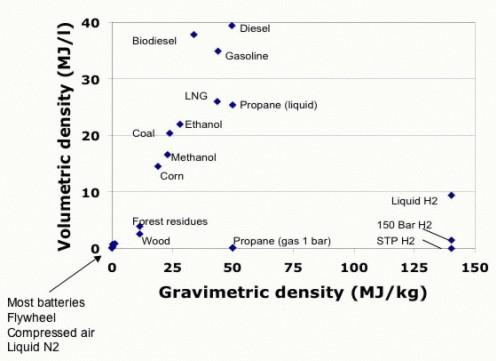
Wykres 1 Energia spalania wybranych paliw przypadających na jednostkę masy i objętości. (2)
W tabeli i na wykresie widzimy zestawienie wodoru ze stosowanymi współcześnie paliwami. Jak widać wodór posiada prawie trzykrotnie większą wartość opałową niż benzyna czy olej napędowy. Wykres pokazuje jednak, że o ile w stosunku masowym wodór o wiele wyprzedza pozostałe paliwa, o tyle w stosunku objętościowym sytuacja jest już zupełnie inna.
Kto prowadzi badania nad pozyskiwaniem wodoru?
- Cywilne ośrodki naukowe, i przykładem może być tutaj Politechnika Lubelska, która prowadzi badania nad wykorzystaniem silnika Renesis wyprodukowanym przez koncern Mazda zbudowanego na patencie Felixa Wankla napędzanego wodorem. Ma być wykorzystany w roli wodorowego agregatu prądotwórczego jako alternatywa dla agregatów benzynowych i Diesla.
- Wojsko.
Dlaczego?
- Ochrona środowiska - która wiąże się bezpośrednio z reakcją spalania wodoru 2H2 + O2 → 2H2O
- Stabilizacja energetyczna - dzięki jego wysokiej wartości energetycznej
Jak się go pozyskuje?
- Elektroliza wody – wodór o dużej czystości ~99,9%
- Reforming parowy gazu ziemnego i gazów towarzyszących rafinacji ropy naftowej
- Technologia plazmowa w temp. 1600-2000°C
- Gazyfikacja węgla lub koksu (analogicznie do reformingu parowego)
- Gazyfikacja biomasy w temp. 800-1000°C (analogicznie do reformingu parowego)
- Piroliza biomasy w temp. 500-700°C
- Konwersja biogazu
- Bezpośrednia biofotoliza wody
- Pośrednia biofotoliza
- Bakteryjne fermentacje beztlenowe np. Rhodobacter sphaeroides
- Fotofermentacje
Chciałbym skupić się głownie na pierwszych dwóch z wymienionych sposobów pozyskiwania wodoru, z uwagi na to, że są dziś najpowszechniej stosowane z uwagi na ilość i czystość otrzymywanego wodoru.
Elektroliza wody
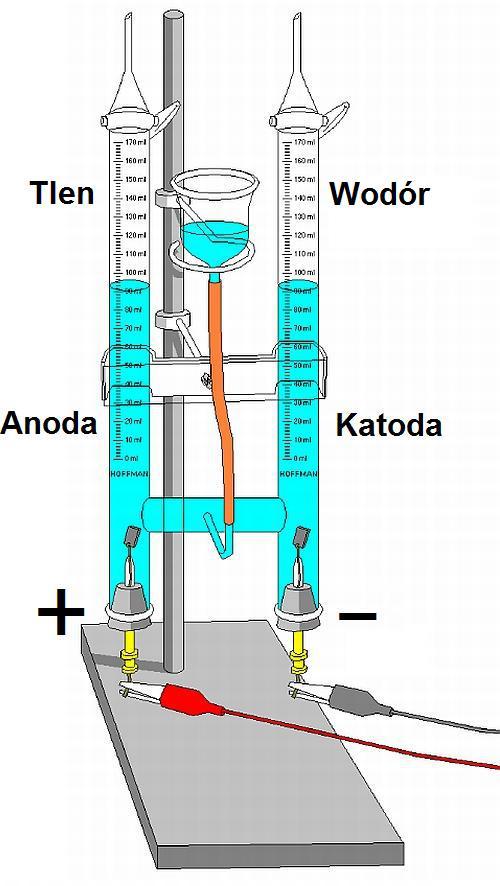
Schemat 1 Elektroliza. (3)
Elektroliza nie należy do skomplikowanych procesów. Reakcje zachodzące podczas elektrolizy to te same reakcje, które zachodzą np. w ogniwie paliwowym typu PEMFC, tyle że w przeciwną stronę. Przykładamy prąd do elektrod odpowiednio + do anody i - do katody. Cząsteczka wody dzieli się na dwa kationy wodorowe i anion tlenowy. Anoda z dodatnim ładunkiem przyciąga ujemnie naładowane aniony, katoda z ładunkiem ujemnym przyciąga dodatnio naładowane kationy, w efekcie czego cząsteczka wody rozbija się na wodór i tlen. Tą metodą uzyskujemy wodór o czystości ~99,9%
Reforming parowy
Reakcja zachodzi w temperaturze 700–1100°C, w obecności katalizatora metalicznego, para wodna reaguje z metanem tworząc gaz syntezowy złożony z tlenku węgla i wodoru CH4 + 2H2O → CO + 4H2
-najpopularniejsza metoda produkcji wodoru
-najtańsza metoda produkcji wodoru
-ilość otrzymanego wodoru na zużytą jednostkę energii jest dużo większa niż w przypadku elektrolizy
Jak się go magazynuje?
-Sprężony w butlach metalowych lub kompozytowych
-Skroplony w butlach kriogenicznych metalowych lub kompozytowych
-Zaabsorbowany z materiałach węglowych
-W postaci fizycznych wodorków metali
-W postaci chemicznych wodorków metali
Wodór sprężony w butlach metalowych lub kompozytowych
- Sprężony gaz przechowywany w temp. ok. 25°C przy ciśnieniu od 15–80 MPa
- 15-35 MPa - systemy mobilne małej mocy (samochody, autobusy)
- 35-80MPa - systemy stacjonarne dużej mocy (elektrownie, systemy CHP – Combined Heat and Power)
Wady:
- Sprężanie = duże nakłady energii
- Mała gęstość wodoru nawet przy dużych ciśnieniach = mała ilość energii użytecznej
- Duża objętości zbiorników i wysoki koszt materiałów w przypadku zastosowań komunikacyjnych znacznie ograniczają zakres działania. Wyjątkiem są autobusy miejskie, które mogą często tankować.
Wodór skroplony w butlach kriogenicznych:
- Gęstość energii jest znacznie wyższa niż w przypadku wodoru sprężonego.
- Trwają badania nad hybrydowymi zbiornikami łączącymi cechy zbiorników kriogenicznych i ciśnieniowych.
Zbiorniki te są:
- lżejsze niż fizyczne wodorki metali
- mniejsze niż zwykłe zbiorniki ciśnieniowe, potrzebują mniejszych nakładów energii do skroplenia wodoru
- wykazują mniejsze straty w wyniku odparowania, niż w przypadku tradycyjnych zbiorników
Wady:
- Skroplenie wodoru wymaga znacznie wyższego nakładu energii
- Musi być on przechowywany poniżej temperatury krytycznej -240,18°C, zazwyczaj w około -250°C
- Ten sposób magazynowania wodoru nie nadaje się do zastosowań, w których wodór nie jest pobierany w sposób ciągły. Wynika to ze strat wodoru poprzez odparowanie.
Zaabsorbowany w materiałach węglowych:
Innym sposobem magazynowania jest wykorzystanie materiałów węglowych m. in. węgle aktywne, nanorurki, aereożele, nanowłókna itp.
Najbardziej popularne są nanorurki. Wodór może wnikać w ich strukturę lub tworzyć warstwę na ich powierzchni. Badania odwracalnej pojemności sorpcyjnej w warunkach ekstremalnych tzn. przy ciśnieniu 10 MPa, i temp. -196°C wykazują wydajność 11.24 % masy zbiornika.
W postaci fizycznych wodorków metali:
Zaadsorbowany na powierzchni niektórych stopów np. LaNi5, czemu towarzyszy wydzielanie się ciepła.
Do odzyskania wodoru trzeba dostarczyć ciepło do zbiornika, a prędkość uwalniania wodoru jest uzależniona od ilości dostarczonej energii. W przypadku małych zbiorników dodatkowe ciepło może nie być konieczne, ale przy większych zbiornikach odzysk gazu może być dużo trudniejszy.
Obecny stan technologii fizycznych wodorków metali umożliwia zmagazynowanie ~5% masy zbiornika.
W postaci chemicznych wodorków metali:
- Magazynowany w postaci związków chemicznych takich jak: CaH2, KH, LiH, NaH, LiBH4, NaBH4
- Reakcja uwalniania wodoru z borowodorku sodu, jest stosunkowo prosta. Wystarczy dostarczyć wody i praktycznie jakikolwiek katalizator, żeby odzyskać wodór.
- Otrzymujemy dwa razy więcej wodoru niż było zmagazynowane poprzez rozbicie cząsteczki wody. NaBH4 + 2H2O → 4H2 + NaBO2
- Borowodorek sodu jest najbardziej rozwiniętą technologią chemicznych wodorków metali
Wykres 2 Charakterystyka zakresów pojemności różnych metod magazynowania wodoru jako gęstość zmagazynowanego gazu w funkcji stosunku do masy zbiornika. (4)
Pojemność magazynowania wodoru w różnych układach:
1) Wodorki metali
2) Mikrokulki
3) Wodór sprężony w pojemnikach metalowych
4) Wodór sprężony w pojemnikach kompozytowych
5) Wodór sprężony w pojemnikach kriogenicznych
6) Wodór ciekły w zbiornikach super zaizolowanych
7) Wodór zaabsorbowany w warunkach kriogenicznych
8) Kulki kompozytowe
Jak widać na zestawieniu poszczególnych metod magazynowania wodoru największą wydajność jak do tej pory uzyskujemy przez przechowywanie skroplonego wodoru w butlach kriogenicznych, a najmniejszą przy magazynowaniu wodoru sprężonego.
Wykorzystanie wodoru jako paliwa:
Ogniwa paliwowe typu:
- PEMFC
- AFC
- PAFC
Silniki spalinowe
- np. Mazda RX-8 Hydrogen
- Magazynowanie energii pozyskanej z innych źródeł np. wiatru
W przypadku ogniw pozwolę sobie całkowicie pominąć ich zasadę działania, ponieważ przebiega ona w ten sam sposób co elektroliza, z tą różnicą że w drugą stronę. Poszczególne typy ogniw różnią się jedynie budową, a w szczególności rodzajem użytej membrany. Skupię się głownie na wadach i zaletach poszczególnych typów tych ogniw.
Ostatniego punktu również nie będę omawiał, ponieważ chodzi w nim głownie o to, że jeżeli nie mamy możliwości odprowadzenia energii np. z farmy wiatrowej położonej na morzu, albo elektrowni fotowoltaicznej na terenie z dala od przesyłowych sieci energetycznych możemy wyprodukowaną w nich energię poświęcić na np. elektrolizę wody otrzymując wodór, który później jesteśmy w stanie przetransportować w pojemnikach tam, gdzie ta energia jest nam potrzebna, czyli np. na stację zasilania wodorem pojazdów samochodowych.
Ogniwa paliwowe typu PEMFC:
Zalety ogniw PEMFC:
· Nieskomplikowana budowa i obsługa - ogniwo składa się z jak mówi nazwa membrany protonowej wykonanej z sulfonowanego teflonu, i dwóch elektrod anody i katody.
· Bezpieczna praca - stały elektrolit
· Niska temperatura eksploatacji
· Łatwy i szybki rozruch
· Szybka reakcja na zmiany obciążenia
· Brak korozji elementów składowych
· Duże moce uzyskiwane z jednostkowej powierzchni geometrycznej w porównaniu z innymi ogniwami
Wady ogniw PEMFC:
· Wrażliwość na CO2, który niszczy elektrolit
· Wysoka cena katalizatorów i materiałów elektrolitycznych
· Krótki czas życia (zaledwie kilkaset godzin)
· Szybko starzejący się materiał polimerowy na membranę
Ogniwa paliwowe typu AFC:
Zalety ogniw AFC to:
- Wysoka sprawność ~89%
- Zastosowanie niedrogich materiałów konstrukcyjnych
- Względnie niedrogie katalizatory reakcji elektrodowych.
Wadami tych ogniw są:
- Wrażliwość na CO2 w dostarczanych gazach, który powoduje przekształcanie KOH do nierozpuszczalnego węglanu (K2CO3), który niszczy porowatą strukturę elektrod i zakłóca podstawową reakcję ogniwa
- Konieczność stosowania H2 i O2 o najwyższej czystości, co eliminuje np. możliwość użycia powietrza atmosferycznego jako źródła tlenu.
Ogniwa paliwowe typu PAFC:
Zalety ogniw PAFC:
- Wyższa tolerancja na CO2 w porównaniu do ogniw AFC i PEMFC
- Względnie prosta konstrukcja
- Wysoka stabilność termiczna i elektrochemiczna
- Ogniwo długowieczne (do 40000 godzin pracy)
- Nie wymaga szczególnego nadzoru i obsługi podczas pracy
- Ogniwa te mogą pracować w skojarzeniu w tzw. systemach CHP generujących prąd elektryczny i wykorzystujących ciepło odpadowe pracy ogniwa np. do celów grzewczych
Wady ogniw PAFC:
- Duża agresywność i korozyjność elektrolitu powoduje niszczenie materiału
- Konieczność wykonania elementów konstrukcji ogniwa z materiałów kwasoodpornych, co podwyższa koszty
- Stosunkowo wolna redukcja tlenu na katodzie powodująca straty w ogniwie
Zastosowanie:
- systemy CHP o mocy 50 - 1000 kW
- systemy energetyczne o mocy 5 - 20 MW
Silniki spalinowe przykład Mazda RX-8 Hydrogen RE:
Silnik Renesis na patencie Felixa Wankla 1300ccm:
- Benzyna 192/231KM
- Wodór 109KM
(Na wodorze silnik pracuje nieco głośniej niż na benzynie)
Zasięg:
5l benzyny = 45km
105l wodoru = 100km
Świeczkowski Paweł
Politechnika Gdańska
Źródła:
www.greenweal.eu
www.archiwum.ekologika.pl
www.ogniwa-paliwowe.info
www.pm.microbiology.pl
www.energieodnawialne.pl
www.kopalniawiedzy.pl
www.wikipedia.org
www.onet.eu
Jan Surygała „Wodór jako Paliwo” WNT Warszawa 2008
Źródła tabel, wykresów i schematów:
1. http://www.bioenergiadlaregionu.eu
2. http://www.ziemianarozdrozu.pl
3. http://www.mt.com.pl
4. http://www.autonawodor.blogspot.com
 |
Autor artykułu:
Planergia |
Planergia to zespół doświadczonych konsultantów i analityków posiadających duże doświadczenie w pozyskiwaniu finansowania ze środków pomocowych UE oraz opracowywaniu dokumentów strategicznych. Kilkaset projektów o wartości ponad 1,5 mld zł to nasza wizytówka.
Planergia to także dopracowane eko-kampanie, akcje edukacyjne i informacyjne, które planujemy, organizujemy, realizujemy i skutecznie promujemy.